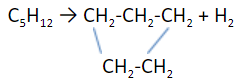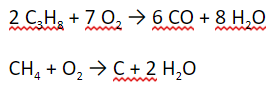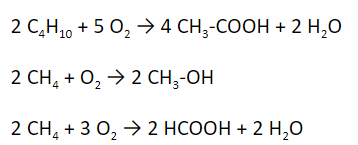Содержание
Алканы (парафины) – линейные органические углеводороды, атомы которых соединены одинарными связями. Они служат топливом для машинных механизмов, а в микробиологической промышленности применяется с целью получения белков.
Изомерия и гомологический ряд
Для алканов свойственны следующие виды изомерии.
- Структурная (по углеродному скелету).
- Пространственная:
- Конформационная (поворотная) – обусловлена возможностью поворота группировок относительно одинарной связи;
- Оптическая – следствие хиральности, т.е. недостатка симметрии относительно правой и левой стороны молекулы.
Гомологи алканов в соответствии с систематической номенклатурой называются по следующей схеме.
- Нахождение главной цепи. Для нее характерно наибольшее количество углеродных атомов.
- Нумерация атомов. Она берет начало с конца, ближнего к заместителю. Если заместители равноудалены, то нумерация начинается со стороны старшего заместителя или оттуда, где их больше. Старшинство соответствует алфавитному порядку (бутил –C4H11 старше, чем пропил –C2H5).
- Название. Сначала присваиваются порядковые номера углеродным атомам заместителей. Если при одном атоме не один заместитель, то номер повторяется несколько раз (например, 3,3-). После этого номера называется заместитель с приставкой. Затем указывается название главной цепи.
Первый представитель гомологического ряда алканов — метан. Его продолжают гомологи метана. Ряд продолжается посредством добавления группы –СН2- к углеродной цепи.
Таблица гомологического ряда и номенклатура алканов
| Формула | Название |
| CH4 | метан |
| C2H6 | этан |
| C3H8 | пропан |
| C4H10 | бутан |
| C5H12 | пентан |
| C6H14 | гексан |
Электронное строение
Имеют форму тетраэдра. Следовательно, гибридные облака одинаковы. Углы между облаками — 109° 28’. Связи одинарны. Атомы углерода в алканах находятся в ![]() -гибридизации.
-гибридизации.
Связь «углерод-углерод» неполярна. Длина ее — 0,154 нм, а энергия – 350 КДж/моль. Данная связь довольно прочная, поэтому реакции проходят в жестких условиях.
Физические свойства
Температуры плавления и кипения зависит от длины молекулы. Чем больше главная цепь, тем температура выше. Первые пять алканов гомологического ряда находятся в газовом состоянии. Углеводороды, содержащие с 5 до 15 атомов, — жидкости. Последующие алканы – твердые.
Газоорбразные и твердые не имеют запаха, в отличие от жидкостей. Все парафины бесцветны и не растворимы в воде.
Способы получения
Алканы в природе находят в:
- природном газе;
- болотном газе;
- рудничном газе;
- горном воске.
Природные смеси трудно разделимы, поэтому есть синтетические метод.
- Восстановление алкил-галогенидов. Реакция идет под действием катализатора.
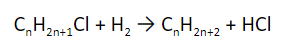
- Гидрирование. Реакция идет под действием катализатора (никеля, платины, палладия)

- Гидролиз магний-органических соединений. Идет в присутствии серной кислоты.
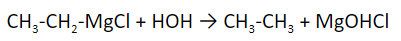
- Реакция Вюрца
Такая реакция сопровождается увеличением углеродной цепи в структурной формуле. Она часто используется для симметричных молекул, т.к. из нескольких исходных веществ получается смесь.
R-Cl + 2 Na + Cl-R’ → R-R’ + R-R + R’-R’ + 2 NaCl
- Реакция Кольбе. Электролиз раствора солей и карбоновых кислот.
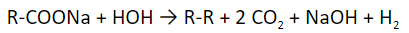
- Синтез Фишера-Тропша. В промышленности из смеси угарного газа и водорода под воздействием температуры, катализатора и давления получают различные алканы.
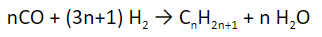
- Реакция Дюма. Декарбоксилирование – процесс отщепления молекулы углекислого газа из карбоксильной (-COOH) или карбоксилатной (-COOMe) группы.
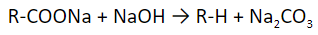
Химические свойства
Алканы – это органические соединения, которым не свойственны реакции присоединения. Для этого класса характерны:
- разложение,
- замещение,
- окисление.
Связь «углерод-водород» разрывается гомолитически, т.е. каждому оторвавшемуся атому достается по одному электрону. В процессе образуются радикалы.
Реакции замещения водорода
- Галогенирование. Данный вид реакции проходит под действием света. Особенностью галогенирования является то, что замещение водорода происходит у наименее гидрированного углерода.

- Нитрование. Эта реакция была открыта в 1888 году ученым Коноваловым. Она проводится с помощью азотной кислоты, концентрация которой 13-14 %, при температуре 140°С.
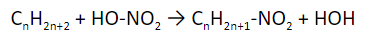
Позднее был разработан метод парофазного нитрования. В нем используется азотная кислота в парах при температуре 250°С.
Это интересно:
Реакции разложения
1. Дегидрирование и дегидроциклизация
Дегидрирование – процесс отщепления водорода. Идет в присутствии никеля, платины, железа.
В реакциях с соединениями из 2-4 атомов углерода рвутся связи «углерод-водород» и образуются углеводороды с кратными связями.
Алканы с пятью и более атомами углерода образуют цикл. Реакции происходят в присутствии платины.
Алканы с углеродной цепью из шести и более атомов образуют замкнутые циклы.
2. Пиролиз метана
Проводится при температуре до 1500°С. Нагревают долго и медленно.
Если нагревать быстро, то образуется ацетилен.
3. Крекинг
Это разложение молекулы на короткие алканы и алкены. Существуют:
- термический – проходит при нагревании без доступа воздуха;
- каталитический – протекает в присутствии катализаторов.
Реакции окисления алканов
Парафины – это малополярные соединения. Не окисляются в нормальных условиях.
1. Горение
Алканы под действием кислорода образуют углекислый газ и воду.
При недостатке кислорода:
2. Окисление под действием катализатора
Это один из способов синтеза уксусной кислоты, метанола или муравьиной кислоты в промышленных масштабах.
Изомеризация алканов
Под действием температуры и катализаторов из неразветвленных парафинов образуются изомеры алканов.
Газообразные алканы используют как топливо, а жидкие – в качестве растворителей. Вазелин – один из представителей твердых алканов. Он широко применяется в медицине.
Алканы в нормальных условиях инертны и их реакции протекают в жестких условиях. Из-за своей предельности им характерны реакции присоединения. Им свойственен радикальный механизм. Алканы – это составная часть нефти, которая применяется во многих сферах. Поэтому парафины имеют большое значение в жизни человека.