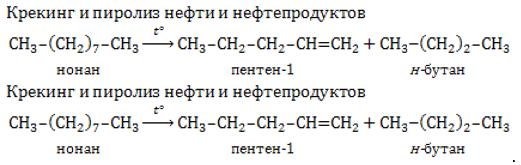Содержание
Пентен – ненасыщенный углеводород ациклического строения, четвертый член гомологического ряда алкенов. Пентен содержится в продуктах нефтепереработки. Вследствие структурных и геометрических отличий в строении молекул одинакового состава пентену присуще свойство изомерии. Изомеры пентена находят применение в производстве топлива и в органическом синтезе.
Строение пентена
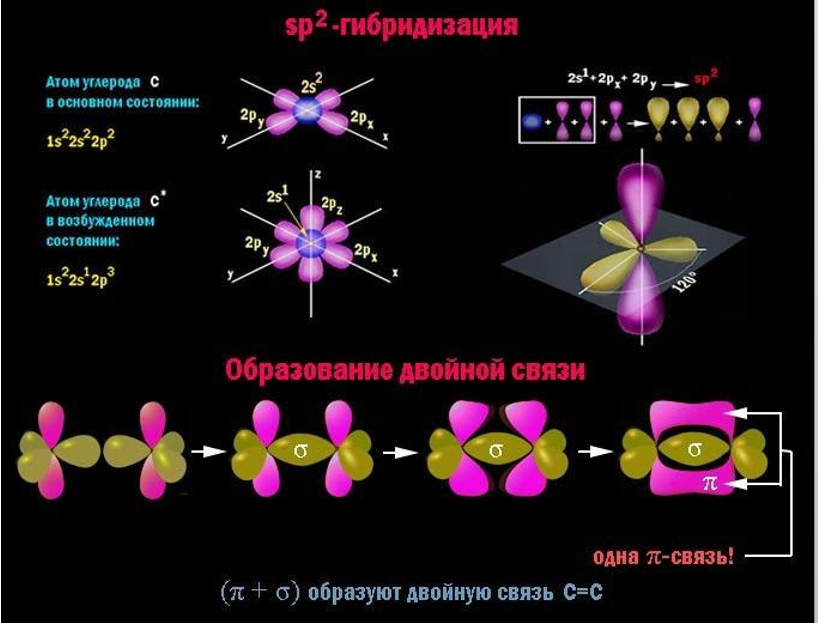
Химическая формула пентена – ![]() . До полного насыщения валентностей углерода молекуле пентена не хватает двух атомов водорода. Гибридизация орбиталей у двух из пяти углеродных атомов принадлежит к типу
. До полного насыщения валентностей углерода молекуле пентена не хватает двух атомов водорода. Гибридизация орбиталей у двух из пяти углеродных атомов принадлежит к типу ![]() , то есть затрагивает не все валентные электроны.
, то есть затрагивает не все валентные электроны.
Гибридные электронные облака, расположенные в одной плоскости с центрами взаимодействующих атомов, вступают в прочную ![]() -связь.
-связь. ![]() -орбитали этих атомов остаются негибридными и путем бокового перекрывания образуют
-орбитали этих атомов остаются негибридными и путем бокового перекрывания образуют ![]() -связь, которая менее устойчива, так как находится вне оси, соединяющей атомные ядра.
-связь, которая менее устойчива, так как находится вне оси, соединяющей атомные ядра.
Сочетание ![]() представляет собой двойную связь
представляет собой двойную связь ![]() , на которую углеродные атомы затрачивают по две свободных валентности из четырех. Поэтому пентен, подобно всем углеводородам ряда алкенов, имеет в молекуле на два водородных атома меньше, чем соответствующие предельные соединения – алканы.
, на которую углеродные атомы затрачивают по две свободных валентности из четырех. Поэтому пентен, подобно всем углеводородам ряда алкенов, имеет в молекуле на два водородных атома меньше, чем соответствующие предельные соединения – алканы.
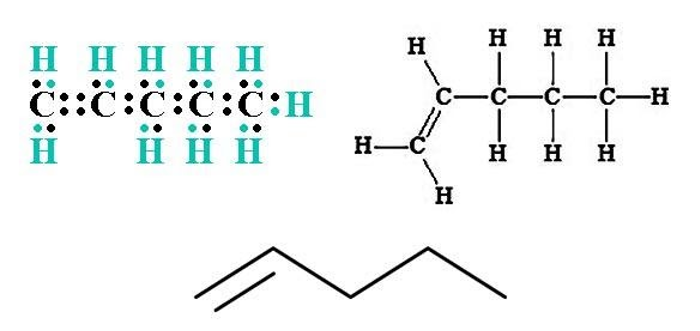
Электронная, структурная и скелетная формулы пентена с простейшей неразветвленной углеродной цепью имеют вид:
Изомерия пентена
Количественный состав молекулы ![]() и присутствие в ней двойной связи обусловливают существование различных вариантов порядка соединения и взаимного расположения атомов.
и присутствие в ней двойной связи обусловливают существование различных вариантов порядка соединения и взаимного расположения атомов.
Структурные изомеры
Структура молекулы определяется позицией, которую занимает в молекуле двойная связь, и формой (ветвлением) углеродного скелета. По этим признакам соединения состава ![]() насчитывают пять изомерных форм:
насчитывают пять изомерных форм:
Межклассовые изомеры пентена
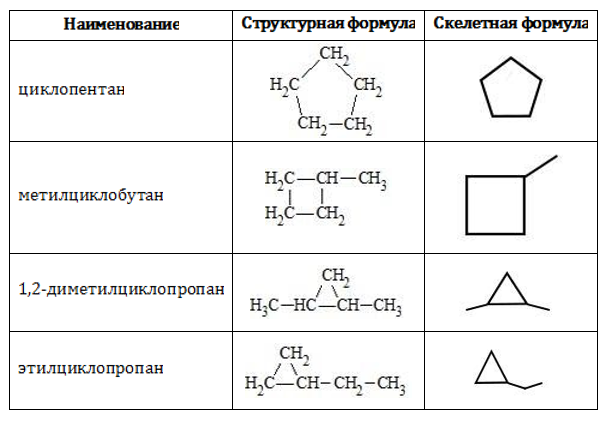
Соединения состава ![]() существуют в классе циклоалканов:
существуют в классе циклоалканов:
Перечисленные в таблице алициклические углеводороды также изомерны пентену.
Это интересно:
Пространственные изомеры
Цис- и транс-изомеры с химической формулой ![]() возникают у пентена-2. Они различаются расположением алкильных и водородных заместителей относительно связи
возникают у пентена-2. Они различаются расположением алкильных и водородных заместителей относительно связи ![]() :
:
Таким образом, у пентена существует шесть изомеров, относящихся к ряду алкенов, и четыре межклассовых изомера из ряда циклоалканов.
Физические свойства
Пентены представляют собой бесцветные, легкие, подвижные жидкости, кипящие при низких температурах. Пары пентенов тяжелее воздуха, в смеси с ним способны образовывать взрывоопасные смеси. Все изомеры, принадлежащие к классу алкенов, имеют общие физические свойства:
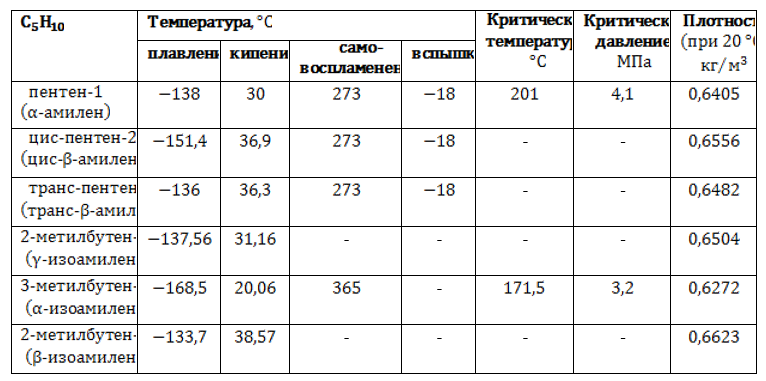
Различия в свойствах, обусловленные особенностями строения изомеров, представлены в таблице:
Химические свойства
Пентены проявляют в химических взаимодействиях все свойства, присущие алкенам.
- Электрофильное (ионное) присоединение:
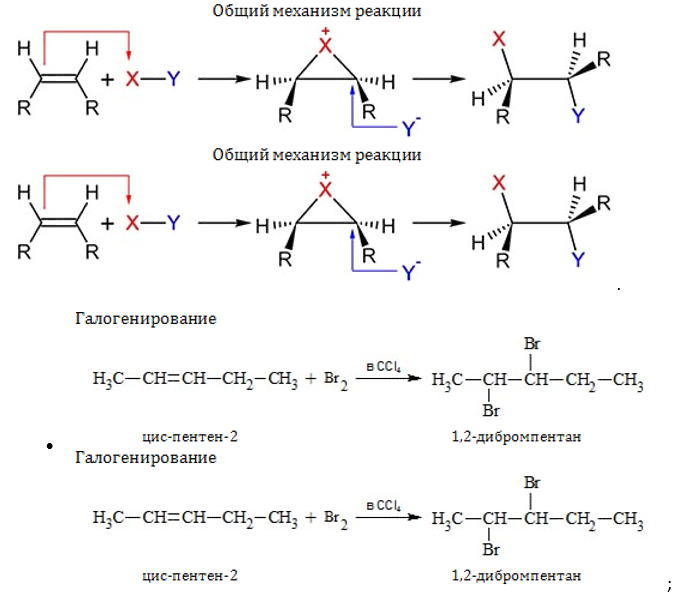

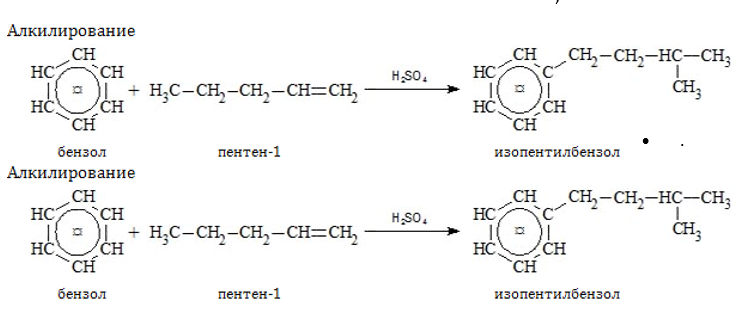
- Радикальное присоединение с разрывом
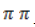 -связи:
-связи:
- Радикальное замещение с сохранением
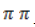 -связи:
-связи: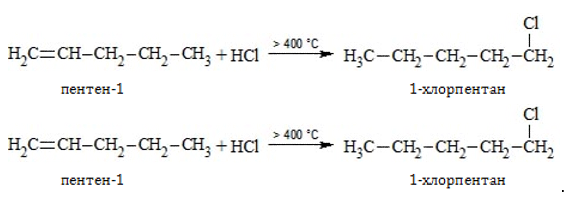
- Окисление:

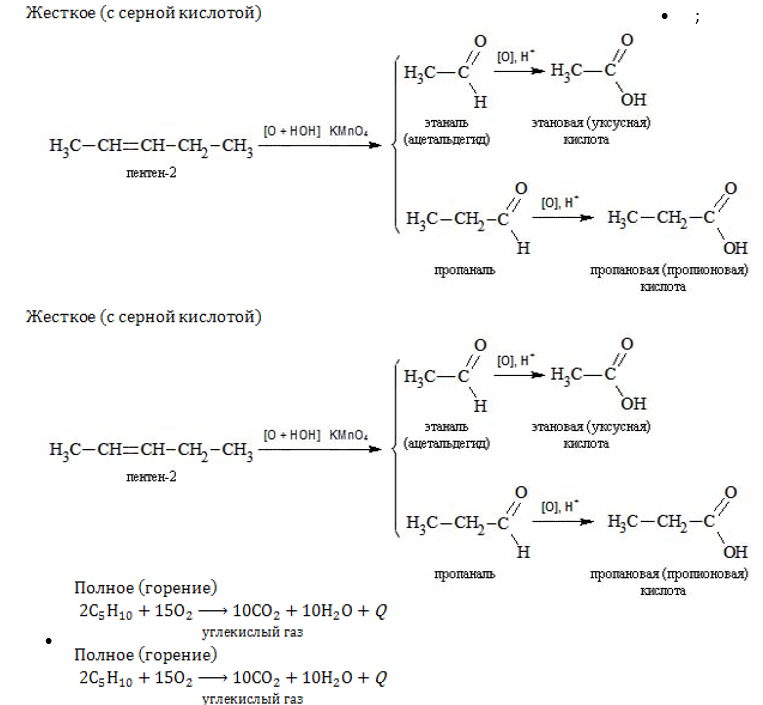
- Изомеризация:

- Полимеризация:
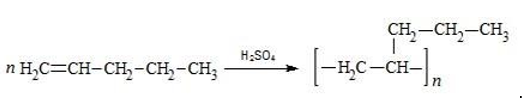
- Разложение:
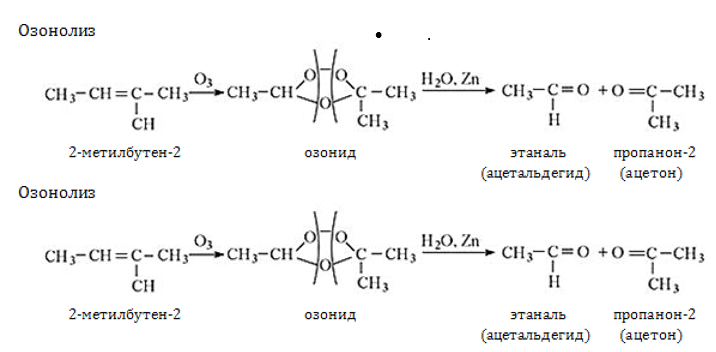
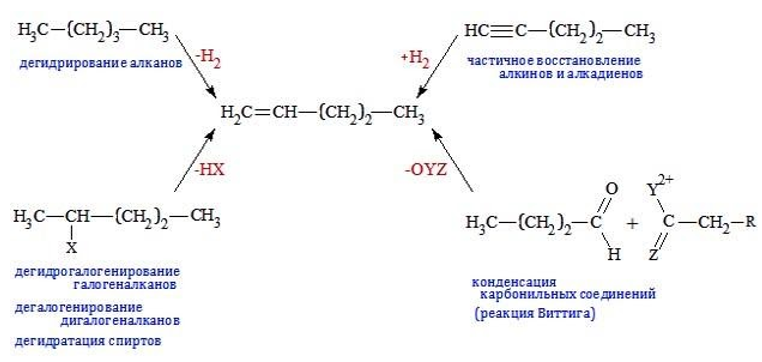
Получение пентенов
Применение пентенов
В промышленности используются все изомеры пентена:
- пентен-1 в составе смеси углеводородов применяется в производстве бензина;
- пентен-1 и пентен-2 используются в синтезе амиловых (пентанолы) и гексиловых (гексанолы) спиртов и соответствующих альдегидов – пентаналя и гексаналя;
- 2-метилбутен-1 и 2-метилбутен-2 применяются в органическом синтезе: получении сложных эфиров, спиртов и изопрена;
- 3-метилбутен-1 находит применение в производстве пластических масс, а также добавляется в состав топлива с целью повышения октанового числа.
Продукты полимеризации пентенов используются в качестве компонентов смазочных масел и типографской краски.
Изомеры пентена в смеси с добавлением изопентана (так называемый технический пентен) служит сырьем для синтеза бутадиена.
При работе с пентенами необходимо использовать средства защиты дыхательных путей и перчатки, так эти соединения оказывают раздражающее воздействие. Поскольку смесь паров пентеновых углеводородов взрывоопасна, следует соблюдать правила техники безопасности.