Содержание
Метан, которым открывается гомологический ряд насыщенных (предельных) углеводородов – алканов – представляет собой наиболее простое органическое вещество. Химические свойства, проявляемые метаном, присущи всем соединениям алканового ряда. Поэтому изучение алканов начинают с рассмотрения структуры молекулы этого вещества и его поведения в химических взаимодействиях.
Общее понятие о строении метана
Определяющая метан формула имеет вид ![]() , то есть молекула его образована одним атомом углерода с валентностью IV и четырьмя водородными атомами. На понимании того, как строится эта молекула, основано дальнейшее изучение всех органических соединений.
, то есть молекула его образована одним атомом углерода с валентностью IV и четырьмя водородными атомами. На понимании того, как строится эта молекула, основано дальнейшее изучение всех органических соединений.
Электроны в атоме углерода
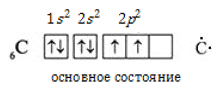
В основном состоянии углерод характеризуется конфигурацией электронного облака ![]()
![]() и валентностью II, поскольку обладает лишь двумя неспаренными внешними электронами:
и валентностью II, поскольку обладает лишь двумя неспаренными внешними электронами:
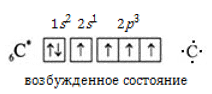
При сообщении некоторой энергии происходит возбуждение атома, 2s2-электроны распариваются и один из них занимает вакантную орбиталь на 2p-подуровне. В результате атом получает четыре неспаренных электрона и валентность IV:
Углерод во всех органических соединениях четырехвалентен.
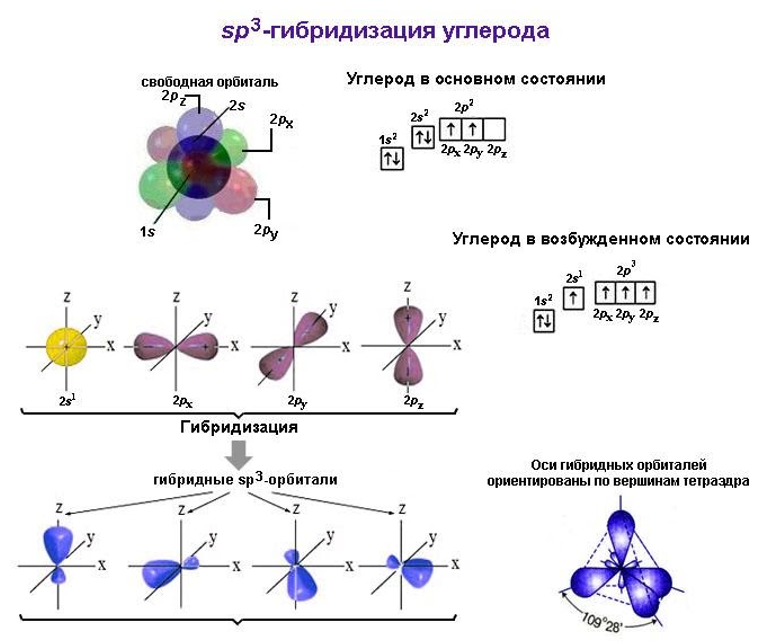
Подуровни 2s и 2p стремятся к выравниванию энергий своих электронов, что ведет к перераспределению электронных плотностей их облаков и к изменению их формы. Образуются гибридные 2sp-облака (орбитали). Их количество зависит от того, сколько орбиталей участвует в гибридизации.
Если в нее вступают наряду с 2s все три 2p-орбитали, говорят о гибридизации типа sp3. В этом случае образуются четыре одинаковых гибридных электронных облака. Оси их вследствие взаимного отталкивания располагаются в пространстве таким образом, что атом приобретает форму тетраэдра. Молекулы метана и прочих алканов образованы только sp3-гибридизованным углеродом.
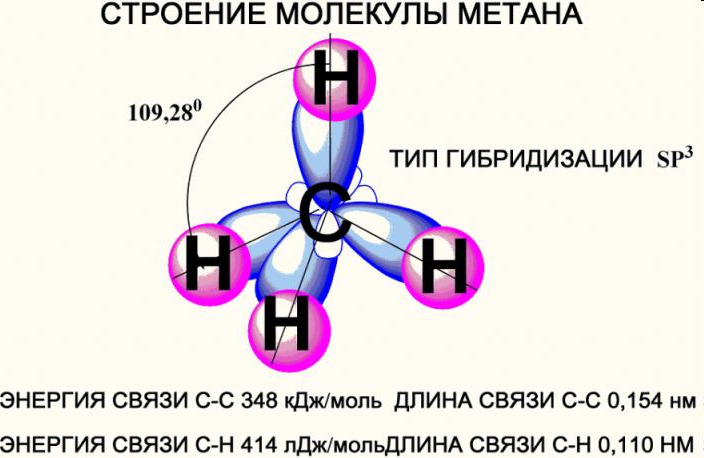
Молекула метана
Углеродный атом в sp3-гибридизованном состоянии вступает в четыре равноправных ковалентных простых σ-связи с водородом. Каждая из них формируется путем перекрывания одной из четырех углеродных 2sp3-орбиталей с 1s1-орбиталью водорода по линии, проходящей через ядра атомов. Ориентация σ-связей соответствует осям гибридных орбиталей, поэтому молекула ![]() имеет тетраэдрическую форму.
имеет тетраэдрическую форму.
Строение молекулы удобно отображать с помощью структурной и электронной формул:
В молекулах метана и его гомологов углерод связывается с наибольшим возможным числом атомов водорода, поэтому углеводороды ряда алканов называют предельными.
Физические свойства
Метан в стандартных условиях (атмосферное давление и температура 0°C) представляет собой газ без цвета и запаха плотностью ![]() (легче воздуха). Основные свойства приведены в таблице.
(легче воздуха). Основные свойства приведены в таблице.
| Наименование параметра: | Значение: |
| Цвет | без цвета |
| Запах | без запаха |
| Вкус | без вкуса |
| Агрегатное состояние (при 20 °C и атмосферном давлении 1 атм.) | газ |
| Плотность (при 20 °C и атмосферном давлении 1 атм.), кг/м3 | 0,6682 |
| Плотность (при 0 °C и атмосферном давлении 1 атм.), кг/м3 | 0,7168 |
| Плотность (при -164,6 °C и атмосферном давлении 1 атм.), кг/м3 | 415 |
| Температура плавления, °C | -182,49 |
| Температура кипения, °C | -161,58 |
| Температура самовоспламенения, °C | 537,8 |
| Критическая температура*, °C | -82,4 |
| Критическое давление, МПа | 4,58 |
| Критический удельный объём, м3/кг | 0,0062 |
| Взрывоопасные концентрации смеси газа с воздухом, % объёмных | от 4,4 до 17,0 |
| Удельная теплота сгорания, МДж/кг | 50,1 |
| Коэффициент теплопроводности (при 0 °C и атмосферном давлении 1 атм.), Вт/(м·К) | 0,0302 |
| Коэффициент теплопроводности (при 50 °C и атмосферном давлении 1 атм.), Вт/(м·К) | 0,0361 |
| Молярная масса, г/моль | 16,04 |
| Растворимость в воде, г/кг | 0,02 |
* при температуре выше критической температуры газ невозможно сконденсировать ни при каком давлении.
Химические свойства
Так как углерод в метане задействует все свободные валентности и молекула максимально насыщена атомами водорода, метан характеризуется слабой химической активностью. В стандартных условиях он не вступает во взаимодействие с щелочами, сильными кислотами, галогенами (за исключением фтора) и щелочными металлами.
Метан участвует в нескольких типах реакций, которые всегда протекают с разрушением углерод-водородных связей ![]() .
.
- Свободно-радикальное замещение:

- Окисление:

- Разложение метана. Наиболее распространенным методом разложения является крекинг, широко используемый в нефтепереработке:

В процессе крекинга происходит разрушение тройной связи в молекуле ацетилена, и среди конечных продуктов реакции присутствуют различные углеводороды.
Метан в природе
В естественных условиях метан имеет несколько источников:
- природный газ и попутные нефтяные газы, в составе которых метан является главным компонентом;
- рудничный газ, поступающий из угольных пластов и образующий с воздухом взрывоопасную смесь;
- вулканические газы;
- продукты обмена веществ некоторых анаэробных микроорганизмов, перерабатывающих клетчатку и обитающих в болотах, стоячих водоемах, в пищеварительном тракте жвачных животных.
Метан способен в больших количествах накапливаться в газогидратной форме в многолетней мерзлоте и на океанском дне. В составе метангидрата молекула ![]() внедряется в полости внутри кристаллической решетки водяного льда. Соединения с такой структурой называют клатратами. При таянии льда газ высвобождается и поступает в атмосферу.
внедряется в полости внутри кристаллической решетки водяного льда. Соединения с такой структурой называют клатратами. При таянии льда газ высвобождается и поступает в атмосферу.
За пределами Земли метан в большом количестве обнаружен на спутнике Сатурна Титане, в атмосферах планет-гигантов и Марса.
Получение метана
В промышленности метан, как правило, не синтезируют искусственно, а выделяют при переработке нефти, нефтепродуктов, очистке природного газа, коксовании каменного угля. В этих процессах метан является продуктом следующих реакций:
Лабораторный синтез метана проводится двумя основными способами:
Области применения
Сфера использования метана включает различные отрасли. Он применяется и как конечный продукт, и в качестве сырья для производства других веществ.
Топливо
Наиболее широко газ используется как дешевый горючий материал в таких областях, как:
- автомобильный транспорт;
- некоторые системы ракетных двигателей (жидкий очищенный метан);
- электроэнергетика (топливо для газовых турбин).
Металлообработка
При горении метана в кислороде развивается температура от 2400 до 2700 °C, поэтому он пригоден для сварки и пайки легкоплавких металлов и сплавов – чугуна, меди, латуни, алюминия. Также он используется как заменитель ацетилена и пропан-бутановой смеси при кислородной резке металлов.
Бытовое применение метана
Во многих регионах метан широко применяется в отопительных системах. Городские сети снабжают значительную часть населения природным газом для кухонных плит.
Метан как химическое сырье
Большую роль метан играет в качестве реагента в процессах синтеза соединений, используемых в разных областях:
- топливная промышленность (получение синтетического бензина);
- производство органических красителей и растворителей;
- производство ацетилена;
- медицина и биология (получение формальдегида – консерванта для биоматериалов).
Читайте также:
Вред и польза метана
Вследствие малой растворимости и слабой химической активности метан нетоксичен, однако длительное пребывание в среде с повышенной концентрацией газа негативно отражается на нервной системе. Если содержание его в воздухе превышает 25%, человек может пострадать от кислородного голодания.
Как сильный парниковый газ, метан оказывает влияние на климат. Несмотря на малую концентрацию в атмосфере, по вкладу в парниковый эффект он занимает третье место после водяного пара и углекислого газа. Парниковое действие метана приблизительно в 25 раз превышает эффект, оказываемый тем же молярным объемом углекислого газа.
Метан обладает полезными свойствами. При полном сгорании он не образует твердых продуктов, загрязняющих внутренние части оборудования и окружающую среду. В сочетании с дешевизной это качество расширяет перспективы использования метана как экономичного и чистого топлива.