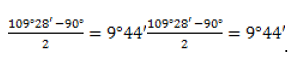Содержание
Среди карбоциклических соединений различают две группы веществ, имеющих принципиально разное строение: алициклические, которые близки по свойствам к соединениям с открытой цепью, и ароматические. Предельные алициклические углеводороды называются циклоалканами, или циклопарафинами. Свойства циклоалканов аналогичны свойствам насыщенных углеводородов линейного строения.
Понятие о циклоалканах. Общая формула
Определяющий признак соединений данного ряда – отсутствие кратных связей в молекулах. Все атомы соединяются посредством одинарных связей, поэтому валентности углерода максимально насыщены.
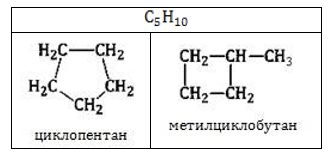
Состав циклоалканов выражает общая формула гомологического ряда ![]() В любом циклоалкане недостает двух водородных атомов по сравнению с алканом
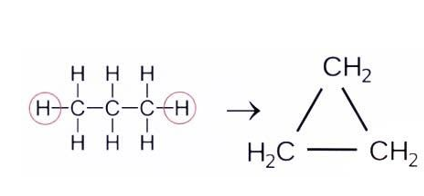
В любом циклоалкане недостает двух водородных атомов по сравнению с алканом ![]() , имеющим такое же количество углерода. Они отщеплены от концевых звеньев линейной молекулы, за счет чего и происходит замыкание углерод-водородной цепочки в циклическую структуру:
, имеющим такое же количество углерода. Они отщеплены от концевых звеньев линейной молекулы, за счет чего и происходит замыкание углерод-водородной цепочки в циклическую структуру:
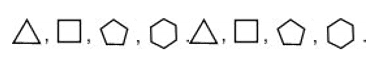
Структурные формулы циклоалканов часто имеют упрощенный вид геометрической фигуры, а запись групп ![]() , расположенных в вершинах многоугольника, опускается:
, расположенных в вершинах многоугольника, опускается:
Строение циклоалканов
Сходство циклопарафинов с алканами проявляется в полном насыщении углеродного скелета молекулы водородом. Оно возникает благодаря тому, что каждый атом углерода формирует по четыре одинарных связи: ![]() либо
либо ![]() и
и ![]() в соединениях с боковыми углеводородными цепочками. Это указывает на тип гибридизации углерода в циклоалканах: sp3.
в соединениях с боковыми углеводородными цепочками. Это указывает на тип гибридизации углерода в циклоалканах: sp3.
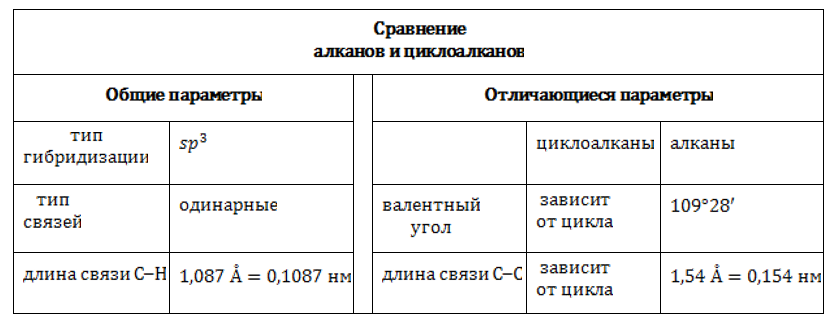
В sp3-гибридизованном состоянии четыре равноценных валентности углеродного атома имеют тетраэдрическую направленность, а величина валентного угла составляет 109°28`109°28`. Но, в отличие от ациклических углеводородов, в молекулах циклоалканов может возникать напряжение, степень которого зависит от числа атомов, участвующих в образовании цикла.
Валентные углы углерода в циклоалканах подчинены геометрии цикла. Связи ![]() отклоняются от нормального направления, вследствие чего и возникает напряжение. Оно, в свою очередь, влияет на прочность молекулы.
отклоняются от нормального направления, вследствие чего и возникает напряжение. Оно, в свою очередь, влияет на прочность молекулы.
Гомологический ряд и устойчивость циклоалканов
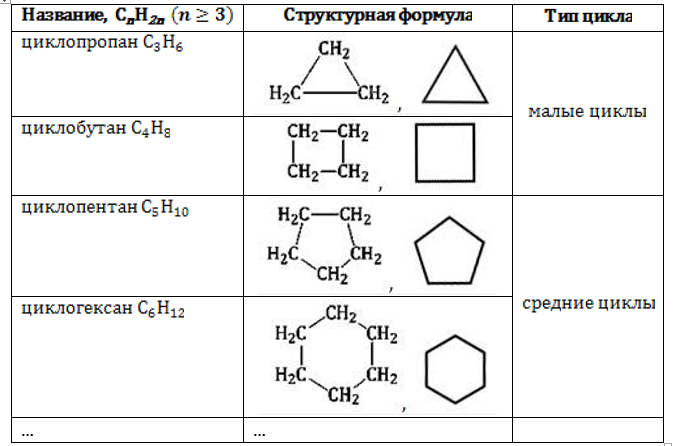
Для образования цикла необходимы как минимум три углеродных атома. Поэтому ряд начинается с соединения ![]() циклопропана. Важной особенностью ряда является внутренняя классификация соединений по типу циклов, от которого зависят их свойства.
циклопропана. Важной особенностью ряда является внутренняя классификация соединений по типу циклов, от которого зависят их свойства.
Малый цикл
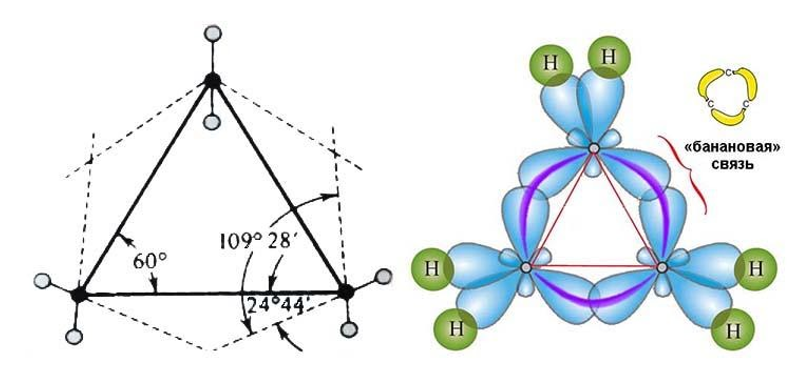
Молекулы соединений малого цикла отличаются сильным угловым напряжением из-за большого отклонения тетраэдрического угла 109°28`109°28`. В трехчленной молекуле циклопропана, где валентные углы в трехчленном цикле должны составлять 60°60°, оно особенно велико:
Это приводит к изгибанию связи, которая из-за характерной формы получила название «банановой». Перекрывание орбиталей в такой связи осуществляется не по прямой между центрами углеродных атомов, поэтому «банановая», или ![]() связь, слабее обычной
связь, слабее обычной ![]() связи.
связи.
Четырехчленная структура циклобутана позволяет ослабить напряжение:
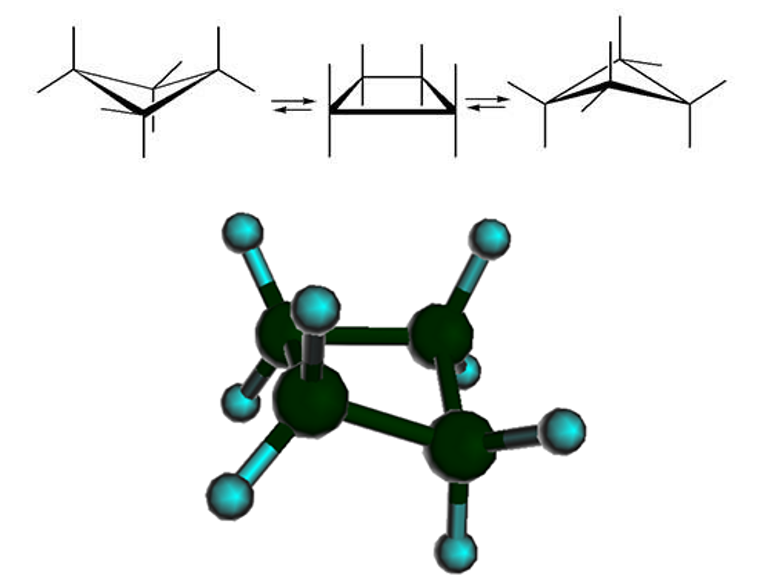
Кроме того, один из четырех атомов в цикле на 25°25° отклоняется от плоскости, в результате чего молекула циклобутана колеблется между двумя равноправными конформациями, условно называемыми «бабочка»:
Средний цикл
Молекулы циклопентана и циклогексана гораздо устойчивее, чем малые циклы, благодаря незначительному отклонению валентного угла:


В циклогексане благодаря большому числу конформаций напряжение отсутствует.
Изомерия и номенклатура
Изомерия циклоалканов может быть двух типов:
- структурная, возникающая вследствие различий в строении;
- пространственная, связанная с вариантами конфигурации одинаковых по строению молекул.
Виды структурной изомерии циклоалканов
- Существование изомеров из разных классов веществ
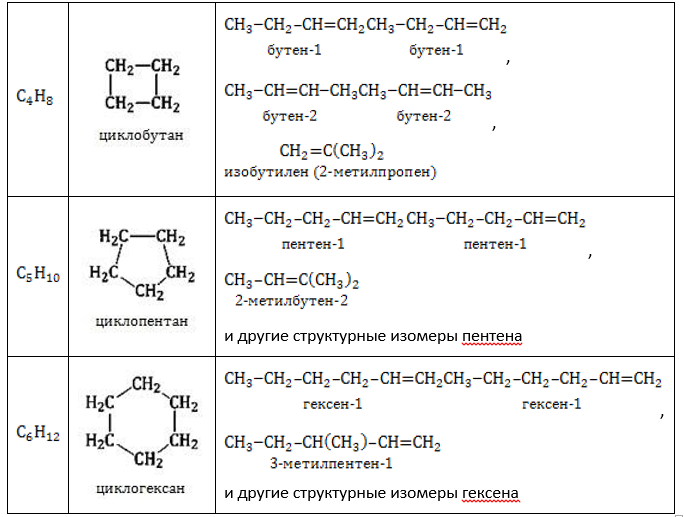
Гомологические ряды соединений, атомный состав которых описывается одной формулой ![]() – алкены и циклоалканы – обладают межклассовой изомерией по отношению друг к другу:
– алкены и циклоалканы – обладают межклассовой изомерией по отношению друг к другу:
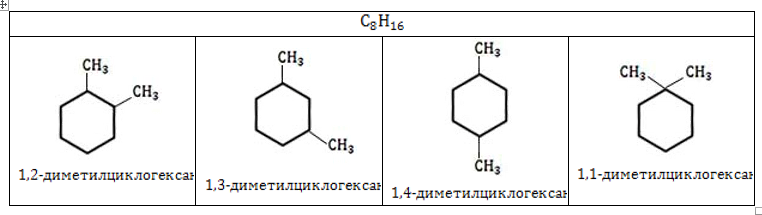
- Изомерия углеродного скелета
Возникновение изомеров данного вида зависит от трех факторов.
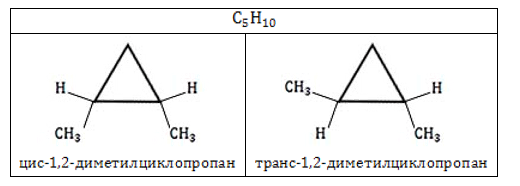
Пространственная изомерия
Циклоалканы способны образовывать геометрические изомеры. Они возникают вследствие невозможности вращения углеродных атомов в цикле вокруг их валентных связей. Положение стоящих при этих атомах радикалов тем самым зафиксировано в пространстве. Заместители у различных углеродных атомов могут находиться либо с одной стороны цикла (цис-изомер), либо с разных сторон (транс-изомер).
Номенклатура
Номенклатура циклоалканов основывается на наименованиях предельных углеводородов открытого строения – алканов. Приставка «цикло-» добавляется к названию алкана с ![]() , равным количеству звеньев в кольце циклоалкана.
, равным количеству звеньев в кольце циклоалкана.
Число радикалов одного состава указывается с помощью приставок «ди-», «три-», «тетра-». Старший радикал обозначается первым, а углеродные атомы нумеруют по наиболее короткому расстоянию между радикалами.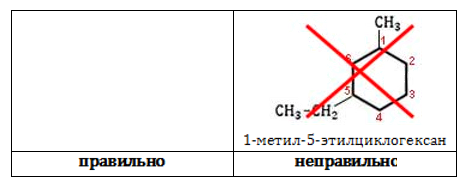
Физические свойства
В целом по физическим свойствам циклоалканы сходны с ациклическими углеводородами предельного ряда. Однако плотность и значения критических температур у них выше, чем у родственных алканов.
Циклопропан и циклобутан в обычных условиях являются газами, циклопентан и последующие шесть членов ряда, включая циклоундекан ![]() – жидкости, а начиная с циклододекана
– жидкости, а начиная с циклододекана ![]() – твердые тела.
– твердые тела.
Химические свойства
Значительные различия между соединениями малых и средних циклов обусловливают разницу в химических свойствах циклоалканов:
- соединения
 менее стойки и охотно участвуют в реакциях присоединения, сближаясь по свойствам с алкенами;
менее стойки и охотно участвуют в реакциях присоединения, сближаясь по свойствам с алкенами; 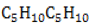 и следующие за ним члены гомологического ряда в проявлении химических свойств аналогичны алканам с таким характерным типом химического взаимодействия, как замещение.
и следующие за ним члены гомологического ряда в проявлении химических свойств аналогичны алканам с таким характерным типом химического взаимодействия, как замещение.
Это интересно:
Способы получения циклоалканов
- Дегалогенирование дигалогенпроизводных предельных ациклических углеводородов. Воздействуя активным металлом, способным отнимать галоген, на дигалогеналкан, можно получить циклическое соединение заданного состава. Условие – наличие между галогенированными группами атомов в цепочке минимум одной группы
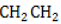 . Реакция получения циклопропана:
. Реакция получения циклопропана: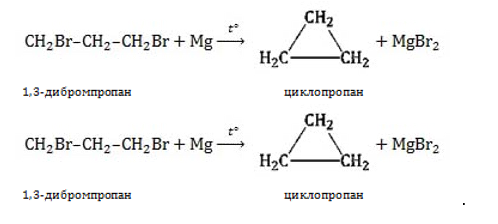
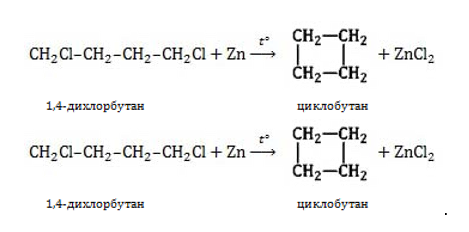
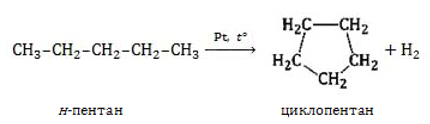
- Дегидроциклизация алканов. При нагревании алканов, содержащих пять и более углеродных атомов, на металлическом катализаторе происходит отщепление водорода (дегидрирование) на концах цепочек с ее замыканием (циклизация алканов):
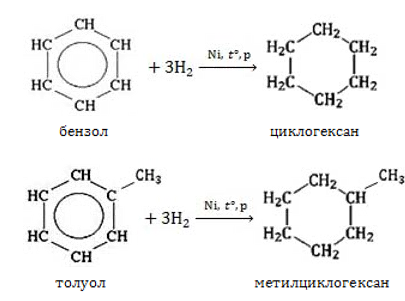
- Гидрирование ароматических углеводородов. Поскольку наименьшее количество углеродных атомов в углеводородах ряда бензола равно шести, этим методом возможно получение циклоалканов не менее чем с шестичленным циклом:
Применение циклоалканов
Наиболее широко используются циклоалканы с углеродным числом ![]() :
:
- Циклопропан применяется в медицинской практике как анестетик, однако из-за повышенной огнеопасности в последнее время его вытесняют другие препараты.
- Циклопентан находит применение в синтезе органических соединений, используется в качестве растворителя, вспенивателя в производстве пенополиуретанов и как заменитель фреонов.
- Циклогексан служит сырьем для производства соединений, из которых получают синтетические волокна капрон и нейлон, для получения ароматических углеводородов. Также его применяют в качестве органического растворителя.
Циклоалканы с более высокими углеродными числами – циклогептан и циклооктан – используются как промежуточные реагенты в синтезе некоторых органических веществ.